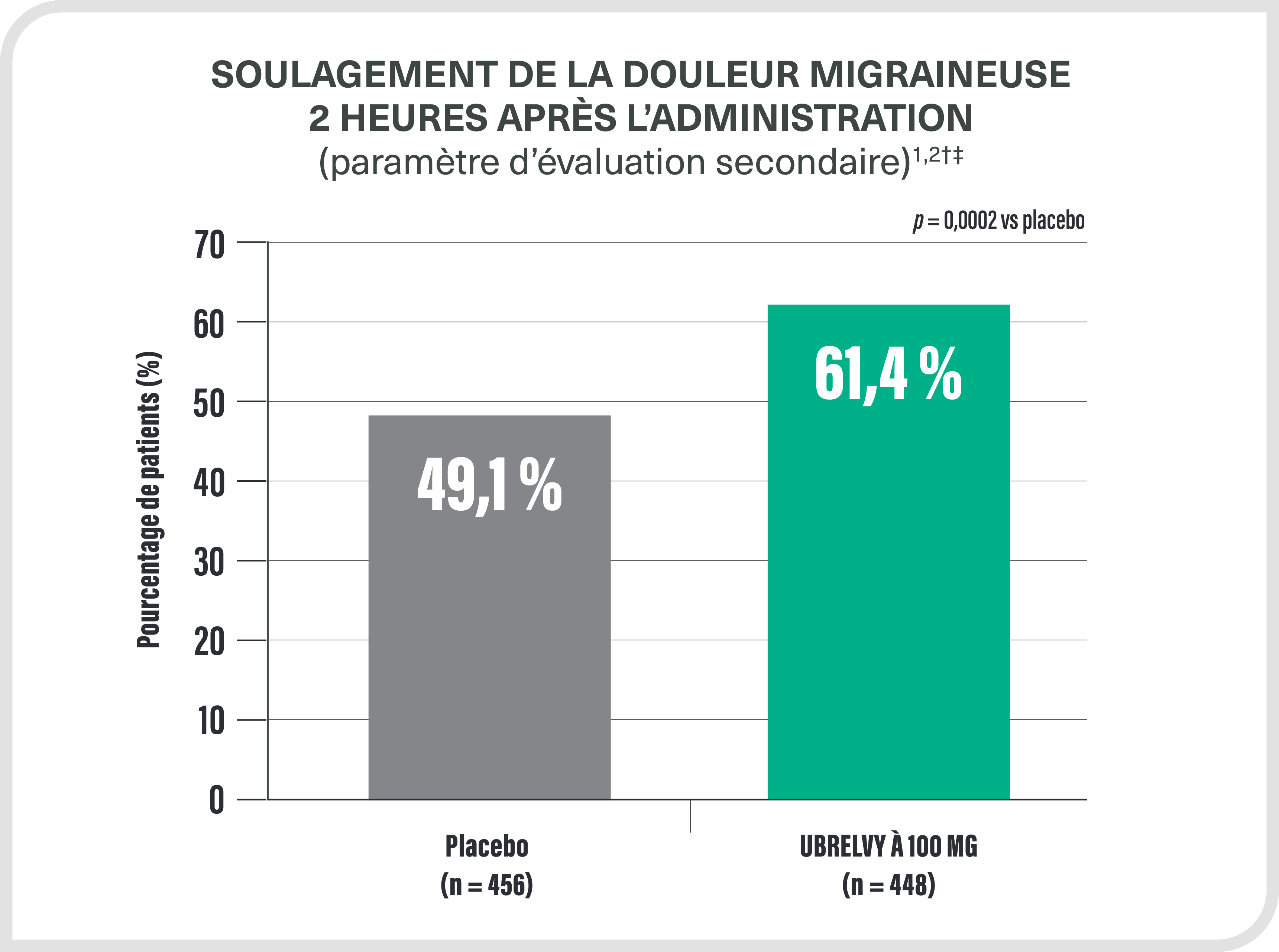
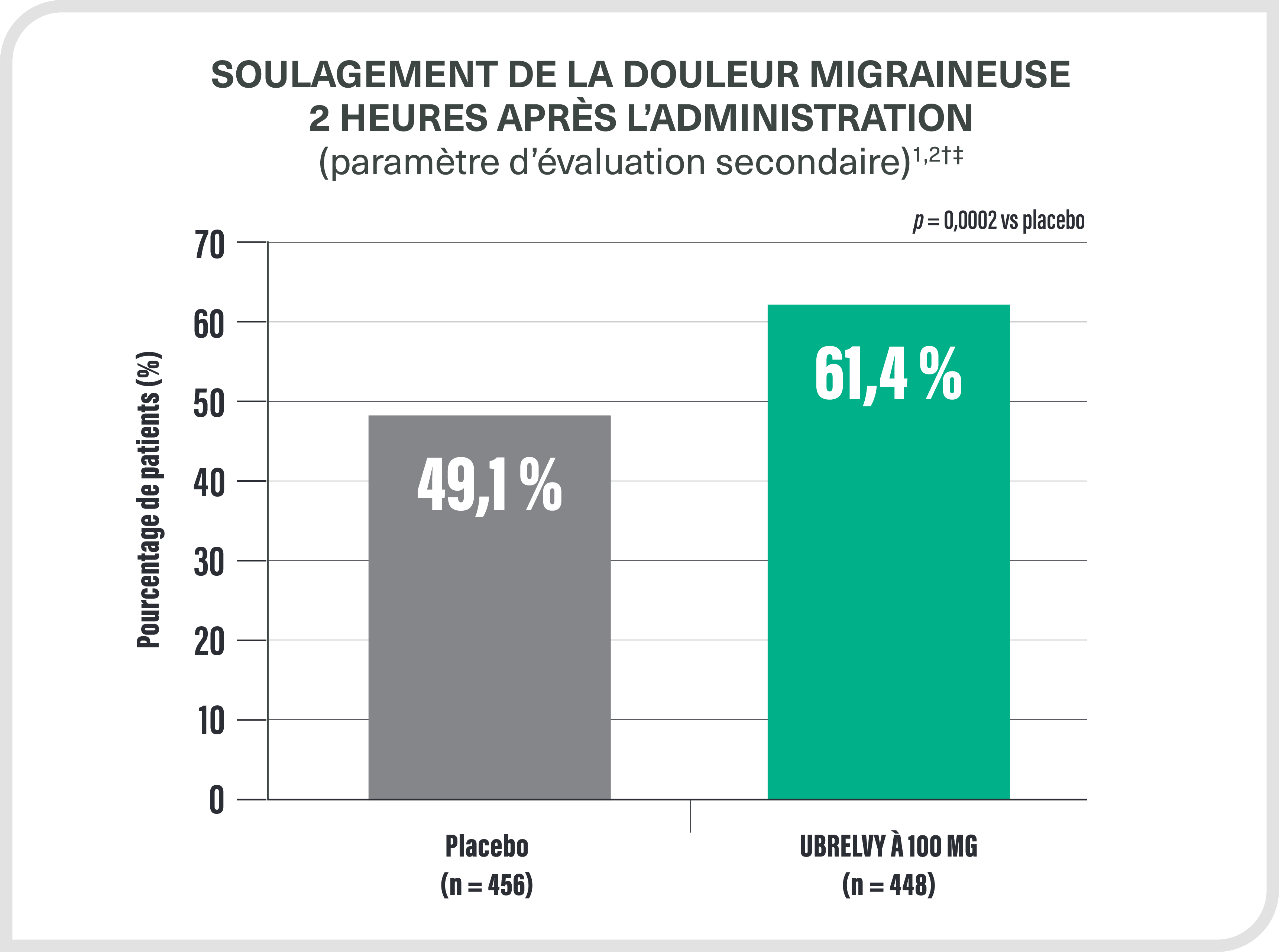
ÉTUDE ACHIEVE I
†Le soulagement de la douleur était défini comme un changement dans l’intensité de la céphalée allant d’une douleur modérée ou intense à une douleur légère ou à l’absence de douleur 2 heures après l’administration de la dose initiale.
‡La population en intention de traiter (ITT) modifiée comprenait tous les patients répartis aléatoirement qui avaient reçu au moins 1 dose du produit expérimental, chez qui l’intensité de la céphalée migraineuse avait été mesurée au départ et chez qui au moins 1 évaluation de l’intensité de la céphalée migraineuse avait été réalisée 2 heures ou moins après l’administration de la dose initiale.
§La suppression de la douleur était définie comme un changement dans l’intensité de la céphalée allant d’une douleur modérée ou intense à l’absence de douleur 2 heures après l’administration de la dose initiale.
Références :
1. Corporation AbbVie. Monographie d’UBRELVY (ubrogépant).
2. Dodick W, et al. Ubrogepant for the Treatment of Migraine. N Engl J Med 2019;381:2230-2241.